神経発生ユニット (政井 一郎)
ユニットの概要

研究
要旨
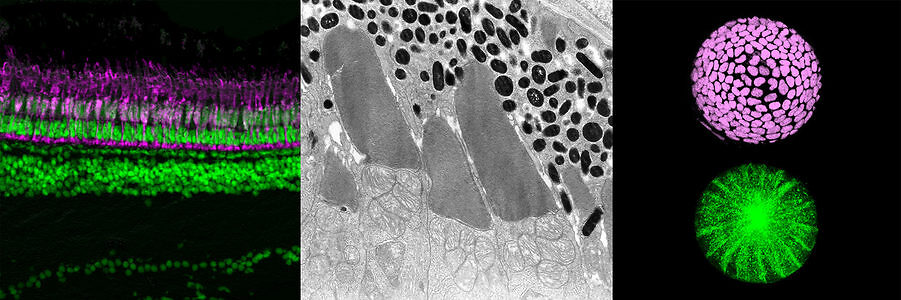
私たちの研究室では、脊椎動物の網膜をモデルに、神経細胞分化、神経回路形成、視細胞変性のメカニズムについて研究している。脊椎動物の網膜は、前脳から眼杯として膨出し、ここには、大きく6種類の神経細胞と1種類のグリア細胞が分化し、視覚情報伝達を担う神経回路を形成する。このような特徴から、網膜は脳における神経細胞分化や神経回路形成を制御するメカニズムを研究する優れたモデルになっている。また、ヒトでは網膜色素変性症に代表される視細胞変性の遺伝病が知られている。最近のヒトゲノム解析の結果、ヒト染色体上に現在307変異遺伝子座がマップされ、そのうち271については原因遺伝子が同定されている。しかし、これらの遺伝子の変異による視細胞変性の仕組みについてはまだ不明な点が多い。
私たちは以前、ゼブラフィッシュを用いた大規模な突然変異体スクリーニングを行い、網膜における細胞分化や神経回路形成、そして水晶体分化に異常を示す約300以上のゼブラフィッシュ突然変異体を同定してきた。現在、これらの突然変異体の原因遺伝子を同定し解析することで、網膜における神経細胞分化と神経回路形成の制御メカニズムを解明するとともに、視細胞変性突然変異体の解析を通して、ヒト網膜遺伝病の解明への貢献を目指している。また、水晶体の線維細胞分化の制御機構も研究している。
References
Chiang, H.-J., Nishiwaki, Y., Chiang, W.-C., and Masai, I. (2024) Male germ cell-associated kinase is required for axoneme formation during ciliogenesis in zebrafish photoreceptors. Dis. Model Mech. dmm.050618. doi: 10.1242/dmm.050618.
Sugiyama, Y., Reed, D., Herrmann, D., Lovicu, F., Robinson, M.L., Timpson, P., and Masai, I. (2024) Fibroblast Growth Factor-induced lens fiber elongation is driven by Rho and Rac. Development 151, dev.202123. doi:10.1242/dev.202123.
Babu, S., Takeuchi, Y. and Masai, I. (2022) Banp regulates DNA damage response and chromosome segregation during the cell cycle in zebrafish retina. eLife. 11:e74611. doi: 10.7554/eLife.74611.
Ahmed, M, Kojima, Y., and Masai, I. (2022) Strip1 regulates retinal ganglion cell survival by suppressing Jun-mediated apoptosis to promote neural curcuit formation. eLife. 11:e74650. doi:10.7554/eLife.74650.
Ranawat, N., and Masai, I. (2021) Mechanism underlying microglial colonization of developing neural retina in zebrafish. eLife. 10:e70550. doi:10.7554/eLife.70550.
Nishiwaki, Y., and Masai. I. (2020) β-SNAP activity in the outer segment growth period is critical for preventing BNip1-dependent apoptosis in zebrafish photoreceoptors. Sci. Rep. 10:17379.
Iribarne, M., Hyde, D. R. and Masai, I. (2019) TNFα induces Müller glia to transition from non-proliferative gliosis to a regenerative response in mutant zebrafish presenting chronic photoreceptor degeneration. Front. Cell Dev. Biol. 7, 296. DOI:10.3389/fcell.2019.00296
Mochizuki, T., Kojima, Y., Nishiwaki, Y., Harakuni, T., and Masai, I. (2018) Endocytic trafficking factor VPS45 is essential for spatial regulation of lens fiber differentiation in zebrafish. Development, 145, pii dev170282.
Iribarne, M. Nishiwaki, Y., Nakamura, S., Araragi, M., Oguri, E. and Masai, I. (2017) Aipl1 is required for cone photoreceptor function and survival through the stability of Pde6c and Gc3 in zebrafish. Sci. Rep. 7:45962.
Mochizuki, T., Luo, Y. J. Tsai, H. F. Hagiwara, A., and Masai, I. (2017) Cell division and cadherin-mediated adhesion regulates lens epithelial cell movement in zebrafish. Development 144, 708 – 719.
Mochizuki, T., Suzuki, S., and Masai, I. (2014) Spatial pattern of cell geometry and cell-division orientation in zebrafish lens epithelium. Biol. Open 3, 982–994.
Imai, F., Yoshizawa, A., Matsuzaki, A., Oguri, E., Araragi, M., Nishiwaki, Y. & Masai, I. (2014) Stem-loop binding protein is required for retinal cell proliferation, neurogenesis, and intraretinal axon pathfinding in zebrafish. Dev. Biol. 391, 94-109.
Mochizuki, T. & Masai, I. (2014) The lens equator: a platform for molecular machinery that regulates the switch from cell proliferation to differentiation in the vertebrate lens. Dev. Growth Differ. 56, 387-401.
Nishiwaki, Y., Yoshizawa, A., Kojima, Y., Oguri, E., Nakamura, S., Suzuki, S., Yuasa-Kawada, J., Kinoshita-Kawada, M., Mochizuki, T., and Masai, I. (2013) The BH3-only SNARE BNip1 mediates photoreceptor apoptosis in response to vesicular fusion defects. Dev. Cell 25, 374 – 387.
Imai, F., Yoshizama, A., Fujimori-Tonou, N., Masai, I. (2010) The ubiquitin proteasome system is required for cell-cycle progression of the lens epithelium and differentiation of lens fiber cells in zebrafish. Development 137, 3257-3268.
Yamaguchi M, Imai F, Tonou-Fujimori N, Masai I. (2010) Mutations in N-cadherin and a Stardust homolog, Nagie oko, affect cell-cycle exit in zebrafish retina. Mech. Dev. 127, 247-264.
Yamaguchi M, Fujimori-Tonou N, Yoshimura Y, Kishi T, Okamoto H, Masai I. (2008) Mutation of DNA primase causes extensive apoptosis of retinal neurons through the activation of DNA damage checkpoint and tumor suppressor p53. Development 135, 1247-1257.
Nishiwaki Y, Komori A, Sagara H, Suzuki E, Manabe T, Hosoya T, Nojima Y, Wada H, Tanaka H, Okamoto H, Masai I. (2008) Mutation of cGMP phosphodiesterase 6alpha'-subunit gene causes progressive degeneration of cone photoreceptors in zebrafish. Mech. Dev. 125, 932-946.
Yamaguchi M, Tonou-Fujimori N, Komori A, Maeda R, Nojima Y, Li H, Okamoto H, Masai I. (2005). Histone deacetylase 1 regulates retinal neurogenesis in zebrafish by suppressing Wnt and Notch signaling pathways. Development 132, 3027-3043.
Masai I, Yamaguchi M, Tonou-Fujimori N, Komori A, Okamoto H. (2005) The hedgehog-PKA pathway regulates two distinct steps of the differentiation of retinal ganglion cells: the cell-cycle exit of retinoblasts and their neuronal maturation. Development 132, 1539-1553.
Masai I, Lele Z, Yamaguchi M, Komori A, Nakata A, Nishiwaki Y, Wada H, Tanaka H, Nojima Y, Hammerschmidt M, Wilson SW, Okamoto H. (2003) N-cadherin mediates retinal lamination, maintenance of forebrain compartments and patterning of retinal neurites. Development 130, 2479-2494.
Masai I, Stemple DL, Okamoto H, Wilson SW. (2000) Midline signals regulate retinal neurogenesis in zebrafish. Neuron 27, 251-263.